Deixar de lado as molestas agulhas que acompanham os diabéticos por muito tempo pareceu um sonho. Agora, está prestes a se tornar realidade, pelo menos parcialmente. Aprovada recentemente pela Agência de Alimentos dos Estados Unidos (FDA), a insulina inalada aparece como uma nova opção para o controle de açúcar no sangue em pessoas que sofrem do tipo 1 da doença, e como um alento a quem tem real pavor às injeções diárias.
Nos EUA, a comercialização do medicamento, que ganhou o nome comercial de Afrezza, deve iniciar em 2015. Por aqui, a expectativa é que, a partir de 2016, possa ser encontrada em farmácias e drogarias.
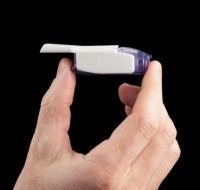
O Afrezza é um pequeno inalador, semelhante a uma bombinha de asma, que contém em seu interior pequenas partículas de insulina. Quando aspiradas pela boca, são absorvidas no pulmão e entram na corrente sanguínea. O medicamente substitui a injeção de insulina de rápida absorção, a maior companheira de quem sofre de diabetes tipo 1 (doença que é desencadeada quando o organismo não produz este hormônio). O medicamento, tanto injetável quanto inalado, é aplicado várias vezes ao dia, sempre antes das refeições, já que quando a pessoa se alimenta, precisa de grandes quantidades de insulina para retirar o açúcar do sangue e transformá-lo em energia.
Assim como na injeção, a empresa MannKind, responsável pelo novo medicamento, afirma que com a inalação os níveis de insulina são alcançados de 12 a 15 minutos após a administração.
Para o endocrinologista Balduíno Tschiedel, presidente do departamento de Diabetes da Sociedade Brasileira de Endocrinologia e Metabologia (SBEM), a aprovação do órgão americano representa um grande avanço no tratamento da doença. Entretanto, ela não livra totalmente os pacientes das temidas injeções, já que existem dois tipos delas, e o novo medicamento substitui apenas um.
— A insulina inalável substitui apenas a injeção de rápido efeito, que deve ser aplicada sempre antes de cada refeição, em uma média de 3 a 5 vezes ao dia. A injeção de efeito lento, que é aplicada em torno de duas vezes ao dia, deve continuar sendo aplicada mesmo com a introdução da insulina inalada — explica o especialista.
Resultados do medicamento a longo prazo são vistos com cautela
A segurança e a eficácia do novo medicamento foram avaliadas em um estudo que contou com mais de três mil participantes que sofriam de diabetes tipo 1 ou 2. A comparação foi feita entre a insulina inalada e a de ação rápida — ambas em combinação com a basal (de ação lenta), durante 24 semanas. O processo foi repetido em comparação com outros tipos de medicamentos antidiabéticos orais, normalmente usados por quem sofre do tipo 2 . Em todos os casos, os resultados da terapia inalada foram satisfatórios.
Os resultados a longo prazo, entretanto, ainda são vistos com cautela por especialistas. O endocrinologista Giuseppe Repetto, chefe do Serviço de Endocrinologia do Hospital São Lucas da PUCRS, explica que entre 2006 a 2007 foi lançada no mercado uma versão de insulina inalada, também aprovada pela FDA. Este medicamento, que acabou sendo comercializado em diversos países, inclusive no Brasil, teve que ser retirado do mercado em poucos meses. Entre os motivos, estavam o tamanho do aparelho (muito maior do que o novo, e que acabou não atraindo os usuários) e o fato de que muitos pacientes apresentaram problemas respiratórios pela inalação do produto.
— A vantagem do novo medicamento é que as partículas são bem menores e, conforme os resultados da pesquisa, não ficam retidas nos bronquios, evitando os problemas respiratórios. Entretanto, somente quando começar a ser comercializada e usada em maior escala poderemos ver se há outros efeitos colaterais — comenta o médico.
Apesar da previsão para lançamento no mercado brasileiro em 2016, a data exata ainda é uma incógnita, já que depende de um pedido da própria indústria à Anvisa para a aprovação aqui no Brasil, o que normalmente ocorre um ano após a circulação do medicamento nos Estados Unidos, prevê Repetto.
